CAR-T: l’antigene intelligente che addestra le cellule a combattere il cancro inzia il suo iter per essere commercializzato in Unione Europea. Arrivate le pre-autorizzazioni dall’Agenzia Europea per i Medicinali (Ema) che consentono l’immissione di CAR-T sul mercato dell’Unione Europea.
LOTTA A DUE TIPI DI LEUCEMIA
La terapia cellulare che usa il sistema immunitario umano nella lotta contro il cancro verrà impiegata per combattere due tipologie di leucemia del sangue: la leucemia linfoblastica acuta (LLA), che rappresenta il 75 % di tutti i casi di leucemia infantile e in Europa ne vengono diagnosticati circa 5.000 casi all’anno, e il linfoma diffuso a grandi cellule B (DLBCL), neoplasia linfoide che colpisce soprattutto, ma non in via esclusiva, soggetti adulti al di sopra del 25esimo anno di età.
PIU’ CHE UN FARMACO, UNA STRATEGIA
Più che di medicinali, gli esperti parlano oggi di una vera e propria strategia terapeutica, visto che si tratta di preparare farmaci ‘personalizzati’: per produrli si manipola geneticamente il sistema immunitario del paziente. Coinvolte nei trial le società Novartis e Kite Pharma. E diverse realtà italiane, come l’istituto nazionale tumori di Milano, l’Ospedale San Gerardo dalla Fondazione Monza e Brianza per il Bambino e la Mamma e l‘Ospedale Pediatrico Bambino Gesù. Monza ha arruolato bambini nel trial registrativo di Novartis, il Bambino Gesù, che però tecnicamente è territorio non italiano, ha presentato lo scorso febbraio il caso di un bambino di 4 anni, affetto da Lla tipo B cellulare, refrattario alle terapie convenzionali, e che a un mese dall’infusione delle cellule programmate non presentava più tracce di cellule leucemiche. A partecipare all’ultimo studio, guidato da Franco Locatelli, anche Airc (Associazione italiana per la ricerca sul cancro), il Ministero della Salute e la Regione Lazio.
L’ITER DI APPROVAZIONE
CAR-T è stato valutato positivamente dal Committee for Advanced Therapies (Cat), e ha poi ottenuto il via libera anche dal Committee for Medicinal Products for Human Use (Chmp). L’Ema lo potrebbe approvare nel giro di pochi mesi e dopo l’ok della Commissione Europea potrà essere commercializzato in Ue e successivamente l’Aifa, (Agenzia italiana del farmaco) lo potrà autorizzare in Italia. L’iter per permetterne l’utilizzo passerà attraverso due fasi di post-autorizzazione distinte. In un primo momento i medicinali verranno inseriti all’interno di programmi sperimentali universitari e di centri qualificati, per poi partire con la somministrazione. I tempi tecnici previsti per sancire l’affidabilità dei trial saranno stabiliti da report cadenzati: per i primi due anni verranno richiesti ogni sei mesi; per i due anni successivi il report sarà annuale e trascorso questo periodo verrà richiesto ogni 4 e 3 anni.
L’ANTIGENE INTELLIGENTE CHE ‘ADDESTRA’ LE CELLULE
La rivoluzione di CAR-T consiste nella capacità di questo ricettore antigene chimerico di riprogrammare le cellule e insegnare loro a riconoscere ed attaccare il cancro. La metodologia con cui è stato progettato prevede che si estragga una quantità di sangue dal paziente, da cui vengono separati i linfociti T, cellule del sistema immunitario che sorvegliano l’organismo e attivano le difese nei confronti dei microorganismi o delle cellule tumorali. Il DNA dei leucociti viene modificato in laboratorio con l’iniezione di CAR, che li manipola e “addestra” ad attaccare le cellule leucemiche.
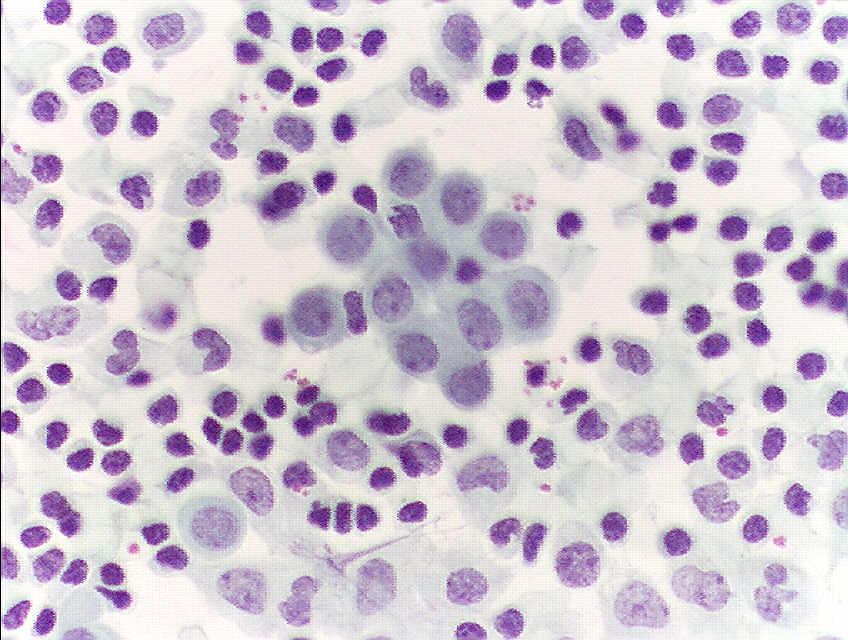
Nel caso di LLA i linfociti vanno incontro a una trasformazione tumorale, in quanto si blocca il loro processo di maturazione e cominciano a riprodursi troppo velocemente invadendo il sangue e arrivando ai linfonodi di tutto l’organismo. Con questa rivoluzionaria terapia possono essere re-infusi nel paziente dopo aver subito una sorta di “ingegnerizzazione”, che li progetta per distruggere la leucemia.
CAR-T è sostenuto da un robusto sistema di raccolta dati effettuato su pazienti registrati. Lo scopo è annotare rischi e benefici, al fine di perfezionare la ricerca. Il trattamento, già in uso negli Stati Uniti ed è stato approvato dalla U.S. Food and Drug Administration (FDA) a ottobre 2017, ha un costo esorbitante di 475mila dollari per il trial Kymriah (Novartis) e 375mila dollari per quello Yescarta (Kite Pharma).
I RISCHI
Gli effetti collaterali della cura sono in qualche modo certi e segnalati anche dal Chmp al rilascio delle autorizzazioni: a causa del rischio di tossicità neurologica, Yescarta in particolare è stato acconsentito nella somministrazione con una strategia di valutazione e mitigazione del rischio, tanto che la FDA richiede che gli ospedali e le cliniche associate che lo dispensano vengano certificati in modo speciale. I possibili rischi includono la Sindrome da rilascio di citochine, che nella sua forma più comune causa complicanze come febbre e tremori, mentre in quella più grave degenera in dispnea grave, infezioni respiratorie e danni neurologici, per questo appare fondamentale lo screening dei trial al fine di monitorare le conseguenze della cura.